L’intelligence artificielle transforme les soins oculaires
L’intelligence artificielle (IA) est appelée à révolutionner de nombreuses industries. Les soins oculaires ne font pas exception, et c’est pourquoi l’Association for Research in Vision and Ophthalmology (ARVO) a récemment organisé un événement en ligne afin d’échanger sur la façon dont l’IA devrait modifier, voire remodeler, les diagnostics rendus et les traitements prodigués.

Au cours de l’exposition technologique de cet événement, Zilia eu l’occasion de présenter son premier produit révolutionnaire nommé Zilia Ocular combinant l’imagerie, la spectrométrie et l’IA et permettant la mesure précise et non-invasive de l’approvisionnement en oxygène dans l’oeil humain, tout cela dans le but d’aider les professionnels de la vue à prévenir, diagnostiquer et prendre en charge les maladies oculaires telles que le glaucome, la rétinopathie diabétique et la dégénérescence maculaire.
Améliorer la précision de l’oxymétrie oculaire grâce à l’IA
Jusqu’à ce jour, la précision a été l’une des lacunes les plus importantes de l’oxymétrie oculaire (c’est-à-dire l’évaluation de la saturation en oxygène dans l’oeil), limitant son usage clinique. La technique algorithmique traditionnelle utilisée pour calculer la saturation en oxygène à partir d’information spectrale est la régression linéaire. Ainsi, le signal lumineux revenant du fond de l’œil du patient peut être assimilé à une combinaison linéaire des spectres de tous ses constituants moléculaires photoabsorbants importants, comme par exemple l’hémoglobine oxygénée et désoxygénée. La régression linéaire vise donc à déterminer la contribution individuelle de chacun de ces constituants. Bien qu’il donne d’assez bons résultats dans l’estimation de la saturation en oxygène, il est sensible à de nombreux facteurs, y compris au bruit, ce qui entraîne une réduction de la précision et de l’exactitude de la mesure. Zilia utilise une nouvelle approche algorithmique basée sur les réseaux de neurones qui s’avère beaucoup plus robuste, permettant des niveaux jamais vus de précision et d’exactitude.
« L’IA a le potentiel d’être utilisée pour le diagnostic précoce et la prise en charge des maladies oculaires telles que le glaucome, la rétinopathie diabétique et la dégénérescence maculaire. »
Qu’est-ce qu’un réseau neuronal convolutif
Un réseau neuronal convolutif (CNN) utilise une opération de convolution pour reconnaître des motifs spécifiques dans, par exemple, un spectre ou signal lumineux. Pour ce faire, un filtre (ou noyau) se déplace de façon itérative dans le spectre de manière convolutive et est comparé au spectre. De cette façon, le réseau apprend à reconnaître un type spécifique de courbe ou de tendance, et retourne un 1 s’il est détecté dans le spectre et un 0 sinon. Cette combinaison de 0 et de 1 s’appelle une carte d’activation (montrée comme la sortie dans la Figure 1) et indique où le réseau a reconnu un certain type de caractéristiques. En convoluant différents filtres à travers le spectre, nous extrayons de multiples types de caractéristiques qui sont combinés pour obtenir la mesure de la saturation en oxygène.
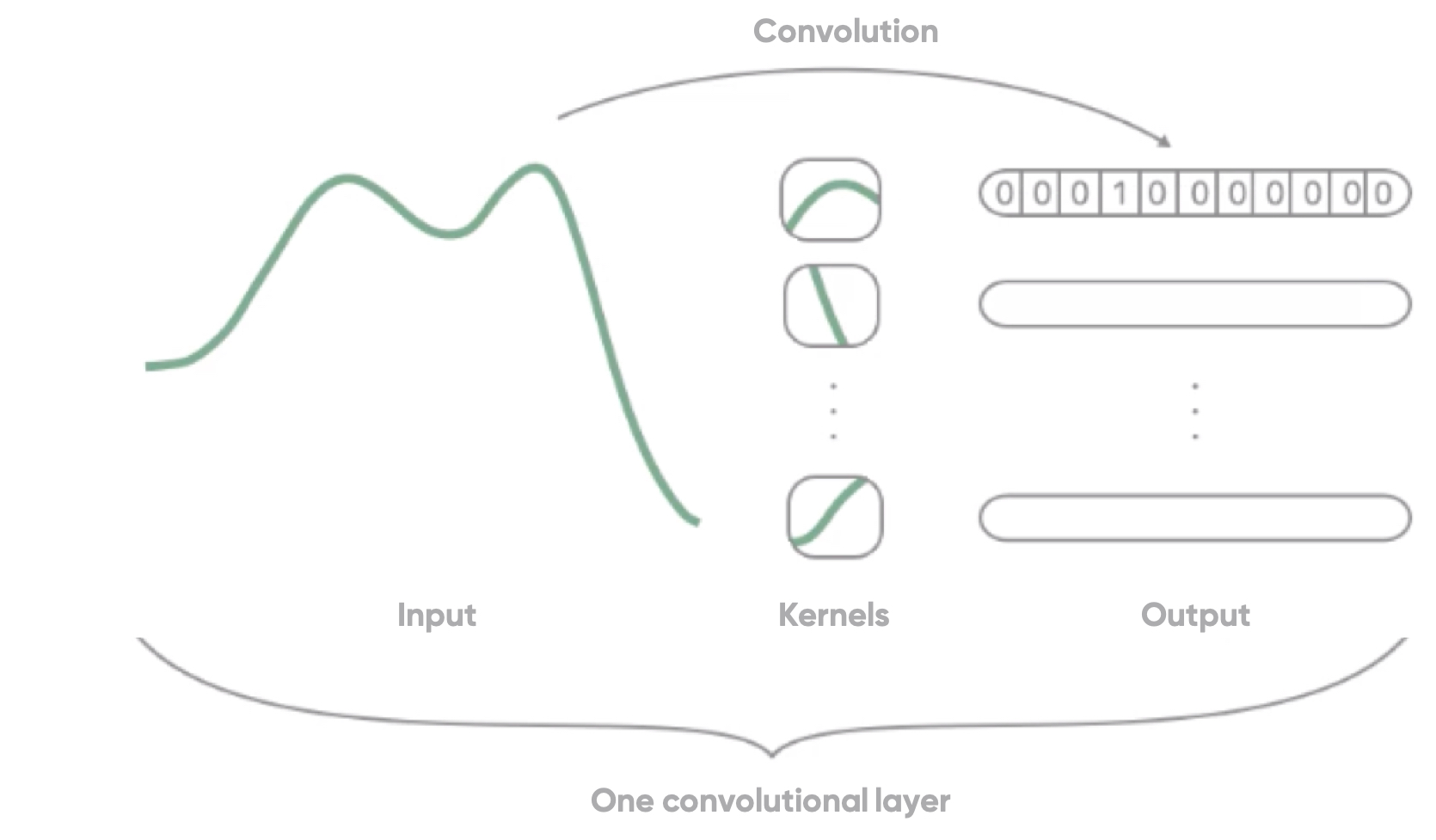
Figure 1 : Schéma d’une couche convolutive dans un réseau neuronal convolutif
Pas de données réelles
Puisqu’il n’existe actuellement aucune façon de mesurer directement et de façon éthique la saturation en oxygène in vivo dans les tissus de la rétine, il n’existe aucune donnée de vérité terrain (ground truth data) pour l’oxymétrie oculaire. D’autre part, de larges quantités de données sont nécessaires pour former un réseau neuronal. Le défi était donc de trouver des moyens novateurs de créer des ensembles de données sur lesquels un réseau pourrait être entraîné et testé.
Création de données simulées
Des spectres lumineux composés peuvent être créés virtuellement en combinant les spectres simulés des différents constituants présents dans le fond de l’œil (Figure 2 ci-dessous), et ce en faisant varier au maximum leur présence théorique. De cette façon, la valeur exacte de la saturation en oxygène devient un paramètre connu et ces données simulées peuvent être utilisées pour former les algorithmes CNN.
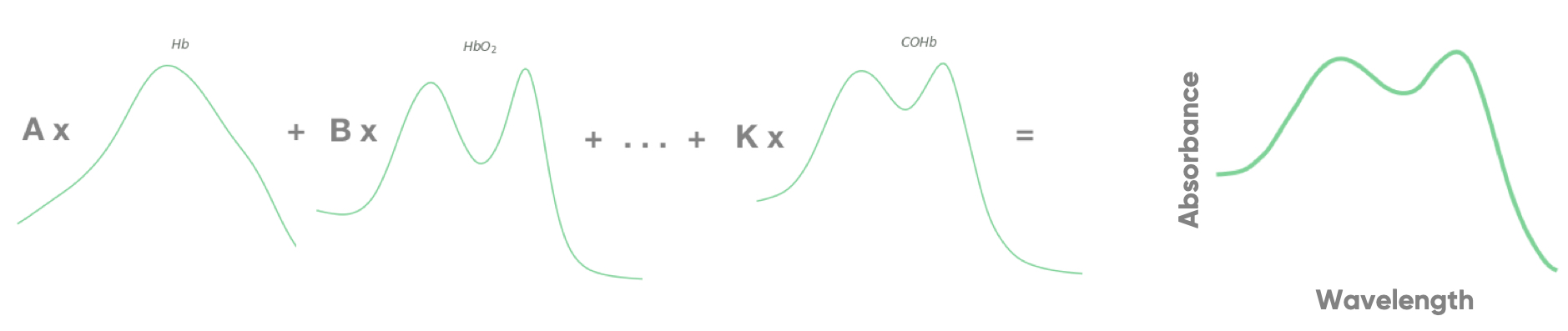
Figure 2 : Spectre simulé créé à partir de la combinaison des spectres des différents composants présents dans le sang
Un œil fantôme, constitué d’un système in vitro imitant les propriétés optiques de l’œil humain et au travers duquel on peut placer du vrai sang oxygéné, peut alors être utilisé pour tester l’algorithme. L’utilisation de cet œil fantôme permet alors de mesurer la saturation en oxygène du sang dans l’œil avec Zilia Ocular et d’autres technologies in vitro reconnues. Conclusion : le CNN utilisé, formé sur les spectres simulés, donne de meilleurs résultats que les techniques d’oxymétrie (in vivo et in vitro) traditionnelles, donnant une erreur moyenne et un écart-type inférieurs aux algorithmes traditionnels basés sur la régression linéaire.
L’IA pour évaluer le mécanisme d’autorégulation oculaire
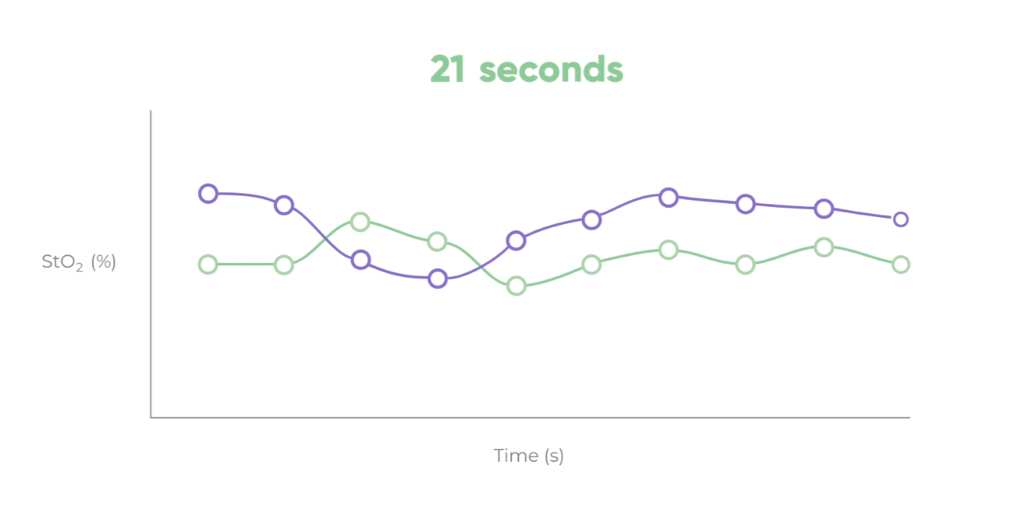
L’autorégulation est le mécanisme adaptatif par lequel le système vasculaire agit en réponse à différents stimuli pour réguler la teneur en oxygène au sein des tissus. Au niveau oculaire comme ailleurs dans le corps, les variations de la saturation en oxygène au fil du temps ou suite à un stimulus peuvent donner des informations très précieuses sur la dynamique de l’autorégulation, sachant que celle-ci peut être altérée dans de nombreuses maladies. En combinant ces informations provenant de différentes caractéristiques du fond de l’œil, Zilia Ocular, propulsée par l’IA, a le potentiel d’être utilisée pour le diagnostic précoce et la prise en charge des maladies oculaires telles que le glaucome, la rétinopathie diabétique et la dégénérescence maculaire. Mais cela pourrait nous amener encore plus loin, en aidant potentiellement au diagnostic et à la prise en charge des maladies cardiaques, neurologiques et neurodégénératives.
L’IA et la vision numérique
Zilia Ocular peut acquérir des données dans n’importe quelle portion du fond de l’œil : l’anneau neuro-rétinien de la tête du nerf optique, la macula, les vaisseaux sanguins ou la rétine. Or, l’IA peut être utilisée pour détecter – et mesurer – automatiquement ces régions à l’aide de techniques de segmentation. De plus, comme on sait que des changements structurels surviennent avec la progression des maladies, l’IA peut fournir un niveau supplémentaire d’analyse pour le diagnostic et la prise en charge des patients. Par exemple, la segmentation des vaisseaux sanguins dans l’œil et leur caractérisation peuvent être considérablement améliorées en utilisant les CNN par rapport aux techniques traditionnelles. Puisque les vaisseaux sanguins oculaires peuvent donner des informations structurelles et fonctionnelles importantes sur la santé vasculaire, la performance de la segmentation est cruciale.
Applications futures pour le diagnostic et la surveillance
L’analyse des images du fond d’œil est à la base de nombreuses techniques diagnostiques classiques, et l’application de l’IA dans ce domaine peut grandement améliorer la puissance analytique. Par exemple, la segmentation et la caractérisation de la rétine peuvent être utilisées pour développer des rapports automatisés de la santé oculaire et évaluent les changements anatomiques dans le temps. Tout cela peut être combiné avec des données métaboliques pour fournir l’évaluation la plus complète et la plus avancée de la santé oculaire qui soit, permettant une détection précoce et une meilleure gestion des maladies oculaires.
Écrit par l’équipe de Zilia le 24 août 2019
Lecture additionnelle
Zilia Ocular homologué par Santé Canada
Ville de Québec, 19 juin 2025 - Zilia est fière d’annoncer l’homologation par Santé Canada de son produit...
Zilia franchit le cap des 1 000 patients enrôlés dans des études cliniques
Québec, le 14 janvier 2025 – Zilia a franchi une étape majeure avec plus de 1 000 patients désormais enrôlés...
Oculomique: Un regard non-invasif sur la santé globale
On dit souvent que les yeux sont le miroir de l'âme, mais ils reflètent tout autant notre santé. On dit...
Solutions



